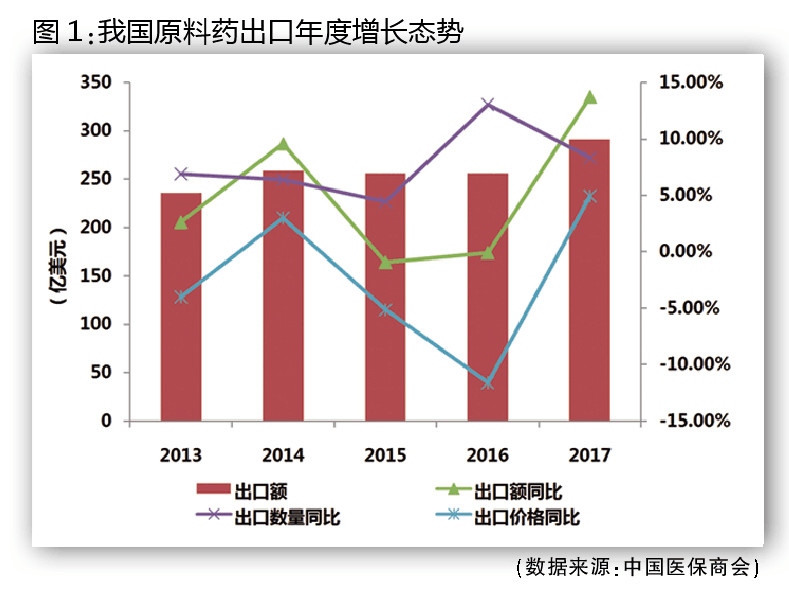
最新數據顯示,2017年,我國化學原料藥制造主營業務收入達到4991億元,同比增長14.68%,相比上一年增速提高了6.28個百分點;原料藥出口額達到291億美元,同比增長13.7%,在經曆兩年小幅調整後重回正增長軌道。
關于2018年年初幾個月的情況,醫保商會從部分原料藥企業了解到,除少數産品因上遊基礎化工原料漲價或缺貨延遲生産外,大部分生産經營活動均在正常進行。
【大環境】
正負能量PK,“回暖”為主基調
正向能量:全球剛需、規範市場、行業升級
全球剛性需求的存在,是維持我國原料藥行業發展的最大動力。目前,全球原料藥市場規模約1500億美元,并仍将以5%左右的速度穩定增長。原料藥市場的剛性需求也體現在我國原料藥的出口上,2015年和2016年,雖然我國原料藥出口額分别同比減少了0.91%和0.06%,但出口數量分别同比增長了4.44%和13.04%,出口數量連創曆史新高,并在2017年繼續增長了8.33%,達到896.15萬噸。
不可否認,我國原料藥行業仍存在大品種産能過剩、小品種壟斷漲價的競争無序問題。國家近年來大力推動供給側結構性改革,主要依托監管和引導的方式逐漸淘汰落後産能,鼓勵原料藥企業轉型升級,同時加大原料藥市場規範力度,打擊違法漲價和惡意控銷行為。
一方面,通過合理提高環保标準,引導龍頭企業提升工藝水平增強競争力,促使高污染不合規的企業退出市場,減少原料藥市場的低價競争者;另一方面,發布《短缺藥品和原料藥經營者價格行為指南》,對惡意操縱原料藥價格的行為進行處罰。
産能的整合、工藝的提升以及合理利潤的保持,将為我國原料藥行業未來的持續
健康發展打下更加堅實的基礎。
不确定因素:各國法規趨嚴、貿易戰
近年來,國内外醫藥監管政策和機構都發生着較大變革。
中國版DMF備案制度開始實施,意味着原料藥的監管不是“放松”了,而是“更嚴”了;美國和歐盟之間的藥品
GMP檢查互認協議已開始運行,這對于正在申請歐美認證的中國原料藥企業而言通過檢查的門檻将更高;印度自去年開始加大了對中國原料藥的現場檢查力度,可以預見出口印度的原料藥未來将遭遇更嚴格的監管。去年美國FDA新局長上任,業界預期FDA将改革監管規範,新的元素雜質要求、藥物共晶監管分類指南等已有所體現。
凡此種種,都對我國生産的原料藥提出了更高的要求,不管是内銷的原料藥還是出口的原料藥。
此外,國際貿易保護主義愈演愈烈,成為我國原料藥國際業務發展最大的不确定因素。美國總統特朗普于近日簽署備忘錄,将依據“301調查”結果對從中國進口的商品大規模征收關稅。美國此後發布的建議對中國征收高關稅的産品清單,其中涉及部分原料藥和
藥品。
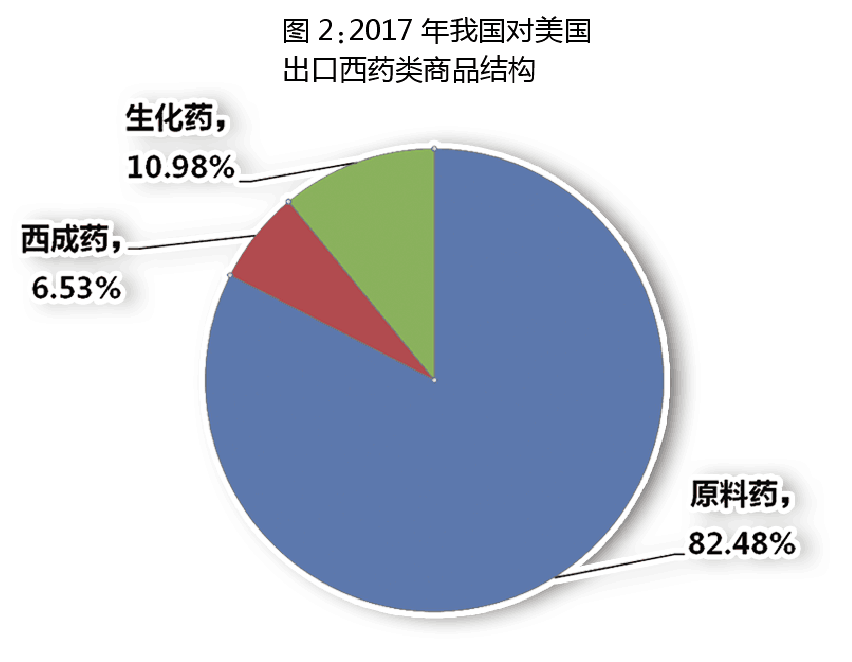
從我國對美國的西藥類商品出口結構看,2017年原料藥出口額達到39.2億美元,占據我國對美西藥類商品總出口額的82.5%,可能會受到征稅波及。印度近年來為扶持本國原料藥産業發展,對我國生産的格列齊特、阿莫西林、氧氟沙星等原料藥産品陸續發起反傾銷調查,并征收反傾銷稅,一定程度上影響了我國原料藥産品對印度的出口,預計未來印度仍将有類似反傾銷調查出現。
【産品說】
劍指原研原料藥、生物原料藥
大宗原料藥:産能産量減少,低價時代一去不複返
我國大宗原料藥産能和産量位居世界第一,這與我國擁有紮實的化工發酵基礎和完善的上下遊産業鍊是分不開的。即便遭遇越來越嚴格的環保監管,部分中小型原料藥企業已經或正在被淘汰,我國仍将繼續在全球原料藥市場占據優勢地位,并且短期内難以撼動。
不過,随着供給側結構性改革的推進,我國大宗原料藥的生産将越來越集中,工藝也會進一步提升。可以預見,未來我國大宗原料藥的産能和産量将有所減少,供求關系趨于平衡,價格和利潤将逐漸恢複到較合理的區間,以往低價的時代将一去不複返,個别原料藥品種甚至存在失去價格競争優勢而轉移到國外的可能。
特色原料藥:産能繼續擴容,目标鎖定專利到期原研藥
以心血管類、抗病毒類、抗腫瘤類等品類為代表的特色原料藥,目标鎖定為專利到期原研藥的仿制原料,科技含量較高,利潤也較豐厚,是我國近十年内發展較為活躍的原料藥闆塊,曾經為華海藥業、創諾
醫藥、江北藥業等
企業的崛起立下了汗馬功勞。
2016年,我國特色原料藥出口額達到35.3億美元,占原料藥的比重達到13.8%。随着近五年内陸續有1940億美元規模的原研藥即将面臨專利到期,越來越多國内企業将目光聚焦于相應的特色原料藥,并提前開始了研發和生産準備工作,預計未來我國特色原料藥的生産和出口規模将繼續擴容和增長。
專利原料藥:我國CMO居全球前列,未來增速20%~30%
在醫藥行業全球化産能合作越來越緊密的大環境下,有些跨國藥企選擇放棄原先的全産業鍊模式,将重心轉移到市場運作上,研發、臨床、生産等環節通過外包來降低成本,專利原料藥應運而生。
原料藥企業接受制藥公司委托,為其專門提供原料藥和關鍵制藥中間體的開發和生産供應服務(即藥品合同生産組織,CMO),例如國内的博騰制藥、凱萊英醫藥、合全藥業、九洲藥業,以及國外的Catalent、龍沙集團、帝斯曼等企業,均走在了行業前列。
據估計,我國CMO市場規模已達50億美元左右,未來還将以20%~30%的速度增長,其中專利原料藥占據較大比重。作為近年來原料藥領域的新熱點,專利原料藥因其較高的利潤受到更多企業的關注,預計未來的開發競争力度将有所增加。
生物原料藥:開發難度大但需求大、潛力大,正蘊釀井噴
與成熟的化學合成或發酵産生的原料藥相比,生物原料藥目前尚處于起步階段。從生産工藝上看,生物制品多數采用生物反應器,菌種來源、工藝變數、雜質種類等不可控因素較多,其原料藥(又稱為原液)質量風險相對較大,因此開發難度也較大。
不過,随着市場對生物藥品的需求不斷增加,生物原料藥市場蘊含着較大的發展潛力,艾伯維、百時美施貴寶、葛蘭素史克等跨國藥企都參與其中,三生國健、奧達生物、百邁博等國内企業也啟動了相關業務。疫苗、幹擾素、重組蛋白、生長激素、單克隆抗體等生物制藥細分産品仍在不斷推陳出新,将推動我國湧現出一批有代表性的生物原料藥企業。